Règle NEXUS (pour National Emergency X-Radiography Utilization Study)
Cinq critères cliniques :
- Douleur en regard des apophyses épineuses
- Déficit neurologique focalisé
- Trouble de la vigilance
- Signe d’intoxication
- Douleur distractive
Pas de critère = pas d’imagerie
Si imagerie nécessaire = faire scanner d’emblée
Références :
Ryken T.C., Hadley M.N., Walters B.C. et al. Radiographic assessment. Neurosurgery, 2013 ; 72 Suppl 2 : 54-72.
Como J.J., Diaz J.J., Dunham C.M. et al. Practice management guidelines for identification of cervical spine injuries following trauma: update from the eastern association for the surgery of trauma practice management guidelines committee. J Trauma, 2009 ; 67(3) : 651-9.
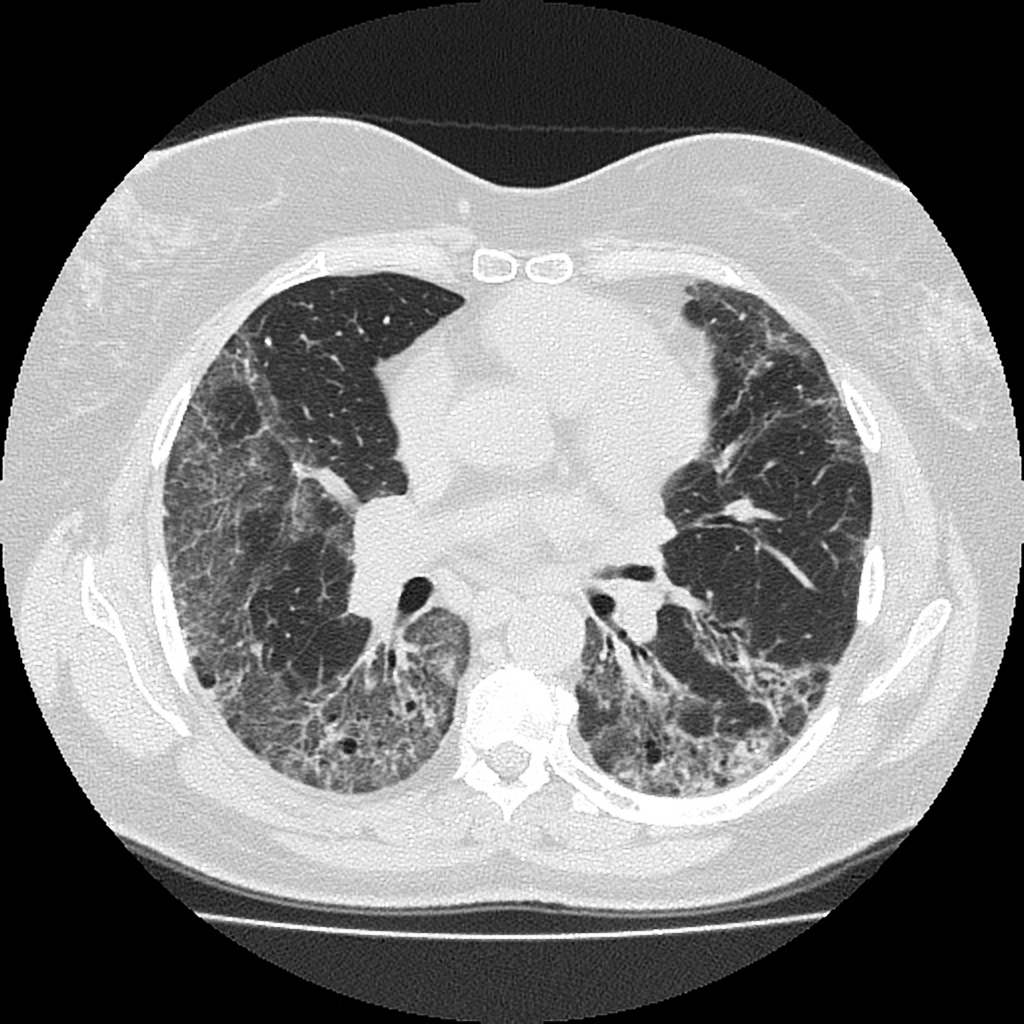
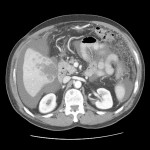
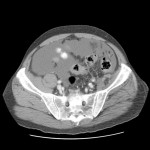
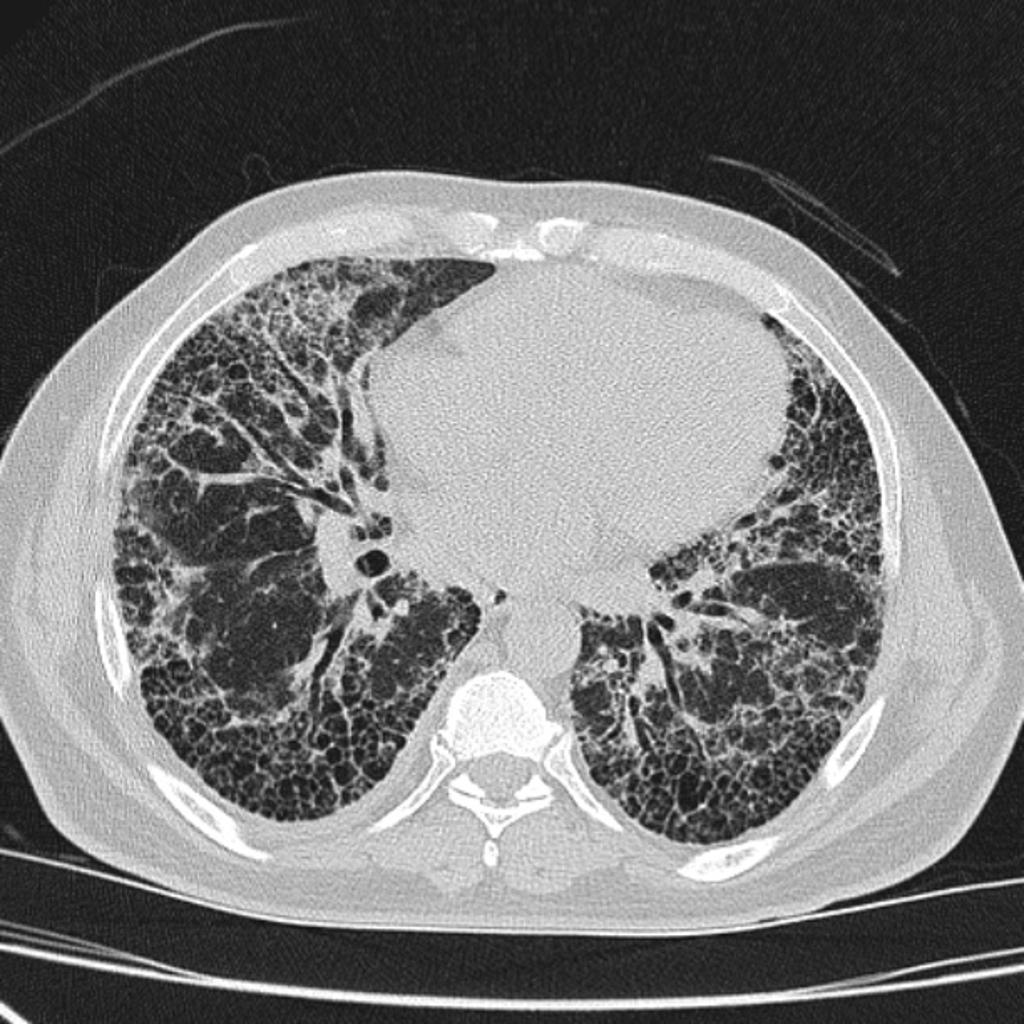 Case courtesy of Dr David Cuete,
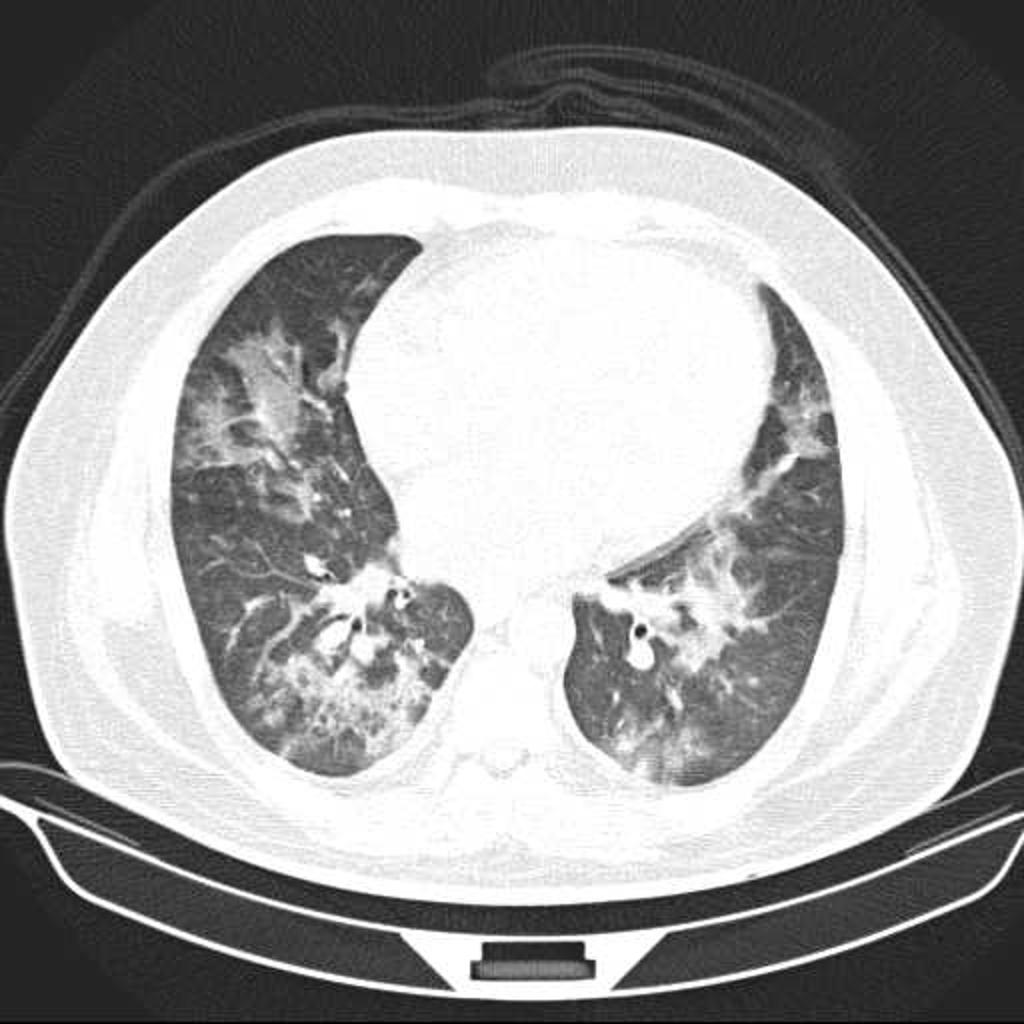
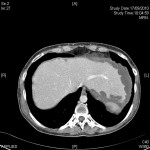
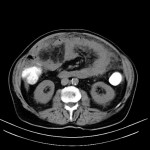
Case courtesy of Dr David Cuete,